پیری و پروتئینها: پیشبینی سن بیولوژیکی و ریسک قلب و کبد

1. مقدمه
پیری یک فرآیند پیچیده و چندعاملی است که با تغییرات ذاتی در سطح سلولی، مولکولی و سیستمیک همراه میباشد. از دههها پیش محققان به بررسی علل و پیامدهای این فرآیند پرداختهاند تا بتوانند عوامل اصلی تسریع در پیری را شناسایی کنند. مطالعات اخیر نشان دادهاند که تغییرات در سطح پروتئینها، به ویژه در سنین میانسالی (تقریباً بین ۴۴ تا ۶۰ سال) نقش مهمی در تعیین سرعت پیری و افزایش احتمال بروز بیماریهای قلبی عروق و کبدی دارند . این مقاله بهطور جامع به بررسی تغییرات پروتئینی در فرآیند پیری پرداخته و ارتباط آن با بروز اختلالات قلبی و کبدی را تحلیل میکند.
یکی از یافتههای بنیادی پژوهشهای اخیر این است که پیری بدن بهطور یکنواخت اتفاق نمیافتد؛ بلکه در نقاط خاصی از زندگی، تغییرات شتاب بیشتری تجربه میشود. به عنوان مثال، در مطالعهای که به بررسی تغییرات پروتئینی در انواع اندامهای بدن پرداخته، مشاهده شده که در حدود ۵۰ سالگی تغییرات شدید پروتئینی رخ میدهد که به نوعی نقطه عطف در فرآیند پیری محسوب میشود . علاوه بر این، مطالعات قبلی نشان دادهاند که پیری ممکن است بهطور ناگهانی در سنین ۴۴ و ۶۰ سالگی تسریع یابد . در ادامه، با استفاده از شواهد موجود، به بررسی دقیقتر این تغییرات و پیامدهای آن خواهیم پرداخت.
2. تغییرات پروتئینی در فرآیند پیری
پژوهشگرانی که به بررسی پروتئوم (مجموعه تمام پروتئینهای یک ارگانیسم) پرداختهاند، نشان دادهاند که پیری بدن با تغییرات قابل ملاحظهای در بیان برخی پروتئینها همراه است. در ادامه به جزئیات این تغییرات پرداخته خواهد شد.
2.1 تغییرات در سطح پروتئینها در سنین میانسالی
مطالعهای اخیر نشان داده است که نمادهای بیومولکولی مربوط به پیری در انواع بافتهای انسانی بهطور قابل توجهی در حدود ۵۰ سالگی تغییر میکنند . از جمله یافتههای کلیدی این پژوهش میتوان به موارد زیر اشاره کرد:
- «توفان مولکولی» در سطح پروتئوم: در حدود ۵۰ سالگی تغییرات بهشدت جهشی در بیان پروتئینهای سلولی رخ میدهد که به نوعی «آبشار مولکولی» محسوب میشود .
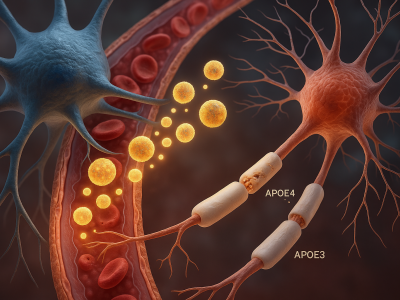
- افزایش بیان ۴۸ پروتئین بیماریزا: این پروتئینها عبارتند از آن دسته پروتئینهایی که با بیماریهای قلبی عروق، کبد چرب، فیبروز بافتی و تومورهای کبدی ارتباط دارند. با افزایش سن، سطح این پروتئینها بهطور چشمگیری افزایش مییابد .
- ارتباط مستقیم با عملکرد اندامها: تغییرات قابل توجه در پروتئومهای اندامهای مختلف مانند قلب، کبد، مغز و عروق نشان دهندهی تغییرات عملکردی در این اندامهاست که میتواند منجر به اختلالات متعدد شود .
2.2 روند پیری در سنین ۴۴، ۵۰ و ۶۰ سالگی
مطالعات پیشین نشان دادهاند که علاوه بر تغییرات شدید مشاهده شده در حدود ۵۰ سالگی، نقاط عطف دیگری نیز در روند پیری وجود دارند. به عنوان مثال:
- سن ۴۴ سالگی: برخی پژوهشها بیان کردهاند که تغییرات بیولوژیکی به شکل اولیه در این سن آغاز میشود که ممکن است بهعنوان علامتی از ورود به دوران میانسالی تعبیر شود .
- سن ۶۰ سالگی: در این سن، تغییرات مولکولی و عملکردی بدنی به حدی صورت میگیرد که بروز علائم بیماریهای مرتبط با پیری، از جمله بیماریهای قلبی و کبدی بهطور فزاینده مشهود میشود .
این نقاط عطف نشان میدهند که پیری یک فرآیند خطی و مداوم نیست؛ بلکه به صورت دورهای و با دورههای تسریع قابل توجه عرضه میشود. در ادامه به بررسی ارتباط این تغییرات با بیماریهای قلبی و کبدی پرداخته میشود.

3. تأثیر تغییرات پروتئینی بر بیماریهای قلبی عروق و کبدی
تحقیقات صورت گرفته نشان میدهد که تغییرات در سطح پروتئینها نه تنها بهعنوان نشانگر پیری عمل میکنند بلکه عامل مستقیم در بروز اختلالات سیستمهای مختلف بدنی، بهویژه سیستم قلبی عروق و کبدی هستند.
3.1 تأثیر بر بیماریهای قلبی عروق
بیماریهای قلبی عروق، به ویژه آترواسکلروز و بیماریهای مرتبط با التهاب عروق، تحت تأثیر تغییرات مولکولی همراه با پیری قرار دارند. از جمله یافتههای مهم در این زمینه:
- افزایش سطوح پروتئینهای التهابی: افزایش سطح برخی از سیتوکینهای التهابی، مانند IL-6، در بدن افراد مسن نشانگر افزایش التهاب سیستمیک است که عاملی کلیدی در توسعه پاتولوژیهای قلبی است .
- اختلالات در متابولیسم لیپیدها: تغییرات در بیان ژنهای مرتبط با متابولیسم گلوکز، لیپیدها و پروتئینهای کلیدی مانند PI3K/Akt، MAPK و NF-κB منجر به اختلال در مدیریت لیپیدها میشود که به نوبه خود خطر بروز بیماریهای قلبی عروق را افزایش میدهد .
- نقش بیومارکرها در پیشبینی ریسک: از طریق اندازهگیری سطح پروتئینهای مشخص در خون، محققان قادر به پیشبینی سن بیولوژیکی و ریسک بروز بیماریهای قلبی برای افراد مسنتر شدهاند .
3.2 تأثیر بر عملکرد کبد
کبد، به عنوان یکی از ارگانهای کلیدی در متابولیسم و سمزدایی بدن، طی فرآیند پیری دچار تغییرات قابل توجهی میشود:
- نشانههای سلولی پیری در کبد: در سلولهای کبدی (هپاتوسیتها) تغییرات ژنتیکی و اپیژنتیکی مشاهده شده که نشان دهنده افزایش ناپایداری ژنومی و اختلال در عملکرد میتوکندری است .
- کاهش اتوفاژی: کاهش فعالیت فرآیند اتوفاژی در کبد افراد مسن باعث تجمع پروتئینهای آسیبدیده و تشکیل غیرقابل تجزیه تجمعاتی مانند لیپوفوسین میشود .
- افزایش تولید سیتوکینهای التهابی: سلولهای کوبفر، که نقش مهمی در پاسخ ایمنی دارند، در کبد پیر سطوح بالاتری از سیتوکینهای التهابی مانند TNFα و IL-6 تولید میکنند که میتواند موجب التهاب مزمن و اختلال عملکرد کبد شود .
3.3 مکانیسمهای التهابی و استرس اکسیداتیو
تغییرات پروتئینی در پیری با افزایش استرس اکسیداتیو و اختلال در مسیرهای تنظیمی مختلف همراه است:
- کاهش پروتئینهای ضد استرس: کاهش سطوح پروتئینهای شوک حرارتی (مانند HSP70، HSP27 و HSP90) که در پاسخ به استرس سلولی نقش دارند، منجر به افزایش حساسیت کبد به آسیبهای ناشی از مواد سمی و دارویی میشود .
- افزایش بار التهابی: تغییرات در بیان پروتئینها باعث افزایش فعالیت سلولهای التهابی میشود که میتواند به بروز التهاب مزمن در عروق و کبد منجر شود .
این مکانیسمها به وضوح نشان میدهند که چگونه تغییرات در سطح پروتئینها میتوانند به عنوان عوامل محرک بروز بیماریهای مختلف در افراد مسنتر عمل کنند.
4. مکانیسمهای مولکولی مرتبط با تغییرات پروتئینی
با توجه به یافتههای ارائهشده، چندین مکانیسم مولکولی کلیدی در ارتباط با تغییرات پروتئینی و پیری شناسایی شدهاند. بررسی این مکانیسمها میتواند بینش کاملی از چگونگی تأثیر این تغییرات بر عملکرد اندامها و بروز بیماریها ارائه دهد.
4.1 تغییرات ژنتیکی و اپیژنتیکی
در سلولهای کبد و سایر اندامها تغییرات ژنتیکی و اپیژنتیکی رخ داده است که به اختلال در عملکرد طبیعی سلولها منجر میشود:
- ناپایداری ژنومی: شواهدی مبنی بر افزایش ناپایداری ژنومی در هپاتوسیتها گزارش شده است که میتواند سبب اختلال در تعمیر DNA و افزایش خطاهای ژنتیکی گردد .
- تغییرات اپیژنتیکی: تغییر در الگوهای متیلاسیون و تغییرات در ساختار کروماتین باعث میشود که برخی ژنها (مانند ژنهای تنظیمکننده متابولیسم و دفاع سلولی) تحت تأثیر قرار گیرند .
4.2 اختلال در اتوفاژی و تجمع پروتئینهای آسیبدیده
اتوفاژی یک فرآیند کلیدی در پاکسازی سلولی از پروتئینها و اندامکهای آسیبدیده است. در طی پیری:
- کاهش اتوفاژی: کاهش فعالیت اتوفاژی در کبد و سایر بافتها منجر به تجمع پروتئینهای آسیبدیده و اوراژنز سطح سلولی میشود که میتواند شاخصی از اختلال در خانهسازی پروتئینی باشد .
- تشکیل تجمعات پروتئینی: تجمع پروتئینهای آسیبدیده مانند لیپوفوسین در سلولها میتواند موجب ایجاد فشارهای استرس سلولی و ایجاد پاسخهای التهابی مزمن گردد .
4.3 افزایش سطوح سیتوکینهای التهابی و استرس اکسیداتیو
تحریک مسیرهای التهابی و افزایش استرس اکسیداتیو از دیگر مکانیسمهای مهم در فرآیند پیری محسوب میشوند:
- افزایش تولید سیتوکینهای التهابی: سلولهای ایمنی مانند کوبفر در کبد در پاسخ به آسیبهای مولکولی، سطوح بالاتری از سیتوکینهای التهابی مانند IL-6 را ترشح میکنند که به نوبه خود باعث التهاب سیستمیک و اختلال عملکرد اندامها میگردد .
- استرس اکسیداتیو: افزایش تولید گونههای رادیکال آزاد به دلیل کاهش فعالیت سیستمهای ضد اکسیدانی در پیری، باعث آسیب به لیپیدها، پروتئینها و DNA میشود؛ این مسأله میتواند روند پیری را تسریع بخشد .
5. تحلیل و بحث دادههای علمی
در این بخش به تحلیل جامع دادههای علمی موجود پرداخته و سعی میکنیم یافتههای مطالعات مختلف را با یکدیگر مقایسه کنیم.
5.1 همآمیختگی یافتههای مطالعات جدید و قدیمی
مطالعهای که نشاندهنده نقطه عطف پیری در حدود ۵۰ سالگی بود، با مطالعات قبلی که پیری را در سنین ۴۴ و ۶۰ سالگی شناسایی کرده بودند، همخوانی دارد .
- در مطالعه جدید، تغییرات شدید پروتئینی در سطح اندامهای مختلف بهعنوان یک «آبشار مولکولی» تشخیص داده شده است که بیان ۴۸ پروتئین مرتبط با بیماریهای انگیزهدهنده (مانند بیماریهای قلبی و کبدی) افزایش مییابد .
- از سوی دیگر، دادههای مربوط به پروتئینهای موجود در خون نشان میدهد که با افزایش سن، تغییرات در سطوح این پروتئینها میتواند سن بیولوژیکی فرد را بهطور دقیقتری نسبت به سن کرونولوژیکی بیان کند .
این همآمیختگی نشان میدهد که استفاده از دادههای پروتئینی میتواند یک ابزار مفید برای پیشبینی روند پیری و نیز تشخیص زودهنگام اختلالات مربوط به آن باشد.
5.2 نقش بیومارکرهای پروتئینی در تشخیص و پیشبینی بیماریها
یکی از چالشهای مهم در پزشکی امروز، پیشبینی بروز بیماریهای مزمن پیش از بروز علائم بالینی است. دادههای ارائه شده نشان میدهد که:
- بیومارکرهای پروتئینی: افزایش یا کاهش میزان برخی پروتئینها میتواند بهعنوان نشانگرهای دقیق پیری و همچنین بروز احتمالی بیماریهایی مانند بیماریهای قلبی عروق و کبدی عمل کنند .
- پیشبینی زودهنگام: اندازهگیری منظم سطح پروتئینهای خون در افراد میانسال، میتواند به تشخیص زودهنگام اختلالات مولکولی، التهابی و متابولیک منجر شود تا در نتیجه مداخلات به موقع صورت گیرد .
5.3 مزایا و محدودیتهای تحقیقاتی
اگرچه دادههای حاصل از مطالعات جدید نویدبخش استفاده گسترده از بیومارکرهای پروتئینی برای پیشبینی بیماریهاست، اما عوامل زیر نیز باید در نظر گرفته شوند:
- تفاوتهای فردی: عواملی مانند ژنتیک، سبک زندگی، رژیم غذایی و شرایط محیطی میتوانند میزان بیان پروتئینها را تحت تأثیر قرار دهند .
- نیاز به مطالعات طولی: برای اثبات پیوستگی میان تغییرات پروتئینی و بروز بیماریهای خاص، مطالعات طولی نظیر پیگیری افراد در طول زمان الزامی است .
- چالشهای فناوری: استفاده از تکنیکهای پیشرفته پروتئومیکس نیازمند تجهیزات گرانقیمت و دانش تخصصی بالا است که ممکن است در برخی از مراکز پژوهشی محدودیت ایجاد کند .
در مجموع، درک دقیق از دینامیک تغییرات پروتئینی در فرآیند پیری میتواند به توسعه راهکارهای تشخیصی و درمانی منجر شود که در نهایت باعث بهبود کیفیت زندگی افراد مسن گردد.
6. پیامدهای بالینی و کاربردهای مداخلاتی
یافتههای علمی مطرح شده اهمیت استفاده از بیومارکرهای پروتئینی در مدیریت و پیشگیری از بیماریهای مرتبط با پیری را نشان میدهد. در این بخش به بررسی پیامدهای بالینی و راهکارهای مداخلاتی بر اساس شواهد پژوهشی میپردازیم.
6.1 تشخیص زودهنگام و پایش پیشرفت بیماری
با توجه به افزایش دقت تشخیص سن بیولوژیکی از طریق اندازهگیری پروتئینهای موجود در خون:
- پزشکان میتوانند با استفاده از آزمایشهای خون مبتنی بر این بیومارکرها، ریسک بروز بیماریهای قلبی عروق و کبدی را پیشبینی کنند .
- پایش دورهای سطوح پروتئینی میتواند نشاندهنده تغییر در وضعیت سلامتی فرد بوده و به عنوان ابزاری برای پیشبینی بروز اختلالات جدی مورد استفاده قرار گیرد .
6.2 مداخلات دارویی و سبک زندگی
با توجه به یافتههای موجود، چندین رویکرد مداخلهای پیشنهاد شده است که میتواند تأثیر قابل توجهی در مدیریت بیماریهای مرتبط با پیری داشته باشد:
- تغییرات رژیم غذایی: مصرف مواد غذایی غنی از آنتیاکسیدانها، پروتئینهای با کیفیت و مدیریت مصرف لیپید، به کاهش استرس اکسیداتیو و کنترل التهاب کمک میکند .
- ورزش و فعالیت بدنی: ورزش منظم نه تنها به بهبود متابولیسم کمک میکند بلکه عملکرد کل سیستم ایمنی را بهبود بخشیده و از بروز التهابهای مزمن جلوگیری میکند .
- رویکردهای دارویی: استفاده از داروهایی که قادر به تنظیم مسیرهای سیگنالدهی مرتبط با استرس اکسیداتیو و التهاب هستند، میتواند روند پیری را کند و از بروز بیماریهای قلبی و کبدی جلوگیری کند .
6.3 استراتژیهای آینده پژوهی
با توجه به نکات مطرح شده، جهت بهبود کاربردهای بالینی لازم است که تحقیقات بیشتری صورت گیرد:
- مطالعات طولی و جامع: پیگیری افراد در طی سالیان متمادی برای بررسی تغییرات مداوم پروتئئوم و ارتباط آن با بروز بیماریهای مزمن، میتواند به ارائه راهکارهای دقیقتر تشخیصی کمک کند .
- توسعه ابزارهای تشخیصی نوین: توسعه سیستمهایی بر پایه تکنولوژیهای نوین مانند پروتئومیکس نسل جدید، میتواند دقت و کارایی تشخیص زودهنگام را افزایش دهد .
- مطالعات میانرشتهای: همکاری میان متخصصان رشتههای مختلف از جمله ژنتیک، بیوشیمی، کاردیولوژی و گوارش، میتواند به درک بهتر پویاییهای مولکولی منجر شود و به طراحی راهکارهای درمانی جامع دست یابد .

7. نتیجهگیری
با توجه به شواهد ارائهشده در این مقاله، میتوان نتیجه گرفت که تغییرات پروتئینی در فرآیند پیری، بهویژه در دوره میانسالی (۴۴ تا ۶۰ سالگی) نقش مهمی در تسریع پیری و افزایش خطر بروز بیماریهای قلبی عروق و کبدی دارد. نکات کلیدی یافتههای این تحقیق به شرح زیر است:
- نقطه عطف پیری: پژوهشهای اخیر نشان دادهاند که در حدود ۵۰ سالگی تغییرات شدید پروتئینی رخ میدهد که میتواند به عنوان یک نقطه عطف در فرآیند پیری محسوب شود .
- افزایش بیان پروتئینهای بیماریزا: افزایش بیان ۴۸ پروتئین مرتبط با بروز بیماریهای قلبی و کبدی در افراد مسنتر مستلزم توجه ویژه به بررسیهای تشخیصی و پیشگیرانه است .
- تأثیرات سیستمیک: تغییرات پروتئینی نه تنها بر عملکرد اندامهای داخلی نظیر قلب و کبد تأثیر میگذارد بلکه باعث افزایش التهاب، استرس اکسیداتیو و ناپایداری ژنومی در سلولها میشود .
- کاربرد بالینی بیومارکرها: شناسایی دقیق بیومارکرهای پروتئینی میتواند به تشخیص زودهنگام، پایش روند بیماری و بهبود نتایج مداخلات درمانی منجر شود .
- نیاز به مطالعات جامعتر: پژوهشهای طولی و مطالعات میانرشتهای برای درک کاملتر دینامیک تغییرات پروتئینی و تأثیر آن بر بروز بیماریها ضروری میباشد .
جدول 2: خلاصه یافتهها و پیامدهای کلیدی
| نکته کلیدی | توضیحات |
|---|---|
| نقطه عطف پیری | تغییرات پروتئینی شدید بهویژه در سن ۵۰ سالگی به عنوان نقطه عطف اصلی در فرآیند پیری شناخته میشود . |
| افزایش ۴۸ پروتئین بیماریزا | ارتقای بیان پروتئینهای مرتبط با بیماریهای قلبی و کبدی در افراد مسنتر که ریسک بروز بیماریهای مزمن را افزایش میدهد . |
| اختلالات متابولیکی و التهابی | تغییرات در بیان ژنها و مسیرهای سیگنالدهی مانند PI3K/Akt و NF-κB باعث اختلال در متابولیسم لیپیدها و افزایش التهاب میشود . |
| کاهش اتوفاژی و افزایش استرس اکسیداتیو | کاهش فعالیت اتوفاژی در کبد و سایر بافتها، موجب تجمع پروتئینهای آسیبدیده و افزایش بار استرس اکسیداتیو میشود . |
| کاربرد بالینی بیومارکرهای پروتئینی | استفاده از ابزارهای تشخیصی مبتنی بر پروتئومیکس جهت پیشبینی سن بیولوژیکی و تشخیص زودهنگام بیماریهای قلبی و کبدی . |
نمودار جریان: مسیرهای مولکولی تأثیرگذار در پیری
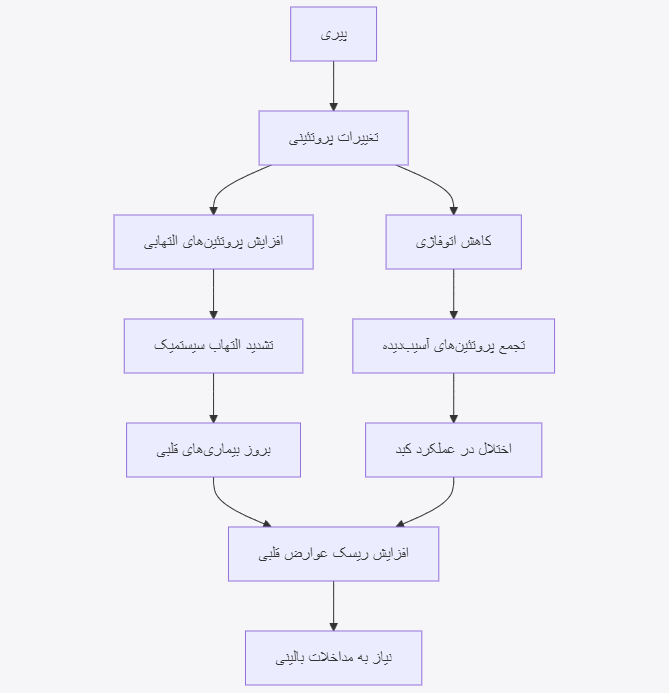
نتیجهگیری نهایی
بر اساس شواهد ارائه شده در مطالعات متعدد، تغییرات سطح پروتئینها یکی از عوامل تعیینکننده در روند پیچیده پیری و بروز اختلالات مرتبط با آن است. شناسایی نقاط عطف زمانی مانند ۴۴، ۵۰ و ۶۰ سالگی نشاندهنده آن است که پیری یک فرآیند یکنواخت نیست، بلکه دارای دورههای تسریع مشخصی در سطح مولکولی میباشد. این یافتهها پیامدهای مهمی در جهت پیشبینی بیماریهای قلبی عروق و کبدی دارند و میتوانند به توسعه ابزارهای تشخیصی و درمانی نوین منجر شوند.
پیامدهای کلیدی به شرح زیر است:
- تأکید بر استفاده از سنجشهای بیومولکولی (پروتئینها) جهت ارزیابی سن بیولوژیکی
- ضرورت انجام مطالعات طولی برای پیگیری تغییرات مولکولی در طی زمان
- کاربرد عملی دادهها در پیشبینی و پیشگیری از بروز بیماریهای قلبی و کبدی
- اهمیت همکاری میان رشتهای برای توسعه روشهای درمانی مبتنی بر تنظیم پروتئومهای آسیبدیده
در پایان، پژوهشهای انجامشده نشاندهنده پتانسیل بالای استفاده از اطلاعات پروتئینومیکس در حوزه تشخیص زودهنگام و بهبود مدیریت بالینی بیماریهای مرتبط با پیری میباشد. این یافتهها میتواند افقهای جدیدی را در علوم پزشکی باز کند و گام موثری در جهت افزایش امید به زندگی سالم و کاهش بار بیماریهای مزمن بردارد.